腺相关病毒(AAV)是基因治疗中最常用的载体,其是非致病性细小病毒,直径约20 nm,无囊膜,基因组长约4.8 kb,其两端为反向重复序列(ITR),对复制、衣壳化等过程有重要作用,中间为rep与cap两个开放阅读框。AAV本身不编码DNA聚合酶,仅依赖宿主细胞或辅助病毒合成自己的基因组,所以无法自主完成复制。AAV在人类和其它灵长类中相当普遍,目前已知有11个血清型,此外,为提高AAV在临床和研究作为载体的效率,开发了许多AAV的人工变型,其在核酸序列,特别是衣壳蛋白的高可变区存在差异,从而导致在基因递送中的不同特性,如全球第1个获批的、基于AAV的产品Glybera®利用AAV1递送脂蛋白脂肪酶(LPL),以治疗LPL缺乏患者。2017年获批的Luxturna®基于AAV2,用于治疗莱伯氏先天性黑蒙,后者导致进行性失明,而2019年获批的Zolgensma®基于AAV9,用于治疗脊髓型肌萎缩(SMA)。
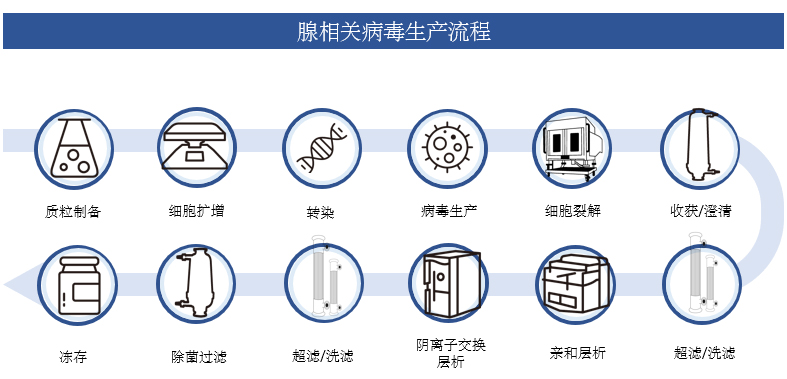
AAV的上游生产有不同的平台策略可选,包括单纯疱疹病毒(HSV)感染、昆虫细胞-杆状病毒表达载体系统以及稳定生产细胞系,但基于HEK293细胞质粒瞬时转染的方法是目前制备临床试验物料的主流方法,其具有更高的适应性且易于使用,前期工程工作量较低,有助于快速启动首次人体研究[3]。基于瞬时转染生产AAV的典型工艺步骤包括:基于贴壁或悬浮培养的细胞扩增、质粒转染、病毒载体生产、细胞裂解、纯化 – 包括澄清、亲和捕获层析、离子交换精纯层析、切向流过滤浓缩/洗滤和最终过滤以及制剂/灌装。
与AV上游策略类似,贴壁 vs. 悬浮培养的选择需根据平台技术能力、所处的开发阶段、目标适应症和给药策略以及预计病毒载体需求量等因素综合考虑,对于患者群体基数较大、需系统性给药或每剂病毒载体含量较高的应用,开发基于悬浮培养的生产策略将更有利于确保所需的规模缩放能力,已有报导实现了高达2,000 L的AAV悬浮培养生产[4]。上游工艺开发的目的是探索病毒生产的最佳条件,包括通过调整转染条件而提高转染效率并确保其在大规模生产条件下的一致性,以及通过优化培养基配方等策略增强病毒生产力、维持病毒感染性。
尽管有些AAV血清型会在培养过程中部分分泌病毒颗粒至细胞培养液中,但为了提高病毒的收率,AAV的下游工艺以在封闭条件下进行的细胞机械或化学裂解以及DNA片段化开始,之后的澄清步骤旨在去除残留的大量质粒DNA以及细胞裂解产生的宿主细胞污染物。澄清过滤器的选择需考虑浊度降低水平、高产物收率以及规模放大的简便性。对于AAV的亲和层析捕获,目前已有针对多种血清型的特异性亲和填料,通常,单步亲和捕获即可达到较高的纯度,但为确保达到特定的杂质去除水平要求,一般结合使用离子交换层析作为精纯步骤。特别是对于AAV生产中分离空衣壳和完整衣壳的挑战,离子交换层析是目前生产规模中最常用的方法。空衣壳被监管机构认为是过程中杂质,需尽可能降低其百分比,并控制空/完整衣壳比例,以确保基因治疗产品的一致性。切向流过滤旨在浓缩产物并置换至合适的缓冲液体系,鉴于AAV较小的粒径,可选择MWCO 100kD的膜组件,而除菌过滤旨在降低微生物负荷,满足所需的无菌性法规要求。
Copyright © 上海多宁生物科技股份有限公司 版权所有 网站地图 | 技术支持: 备案号:沪ICP备20017026号-2
备案号:沪ICP备20017026号-2
留言框-